
土耳其卫生署正规授权
全球药品进出口批发商


全球药品进出口批发商

 FDA 已批准纳武单抗与伊匹单抗联合治疗
FDA 已批准纳武单抗与伊匹单抗联合治疗
根据 3 期 CheckMate-8HW 试验的数据,纳武单抗和伊匹单抗的组合疗法已获得 FDA 批准用于治疗转移性结直肠癌。...
查看详情 FDA批准Alpha DaRT治疗复发性胶质母细胞瘤的IDE申请
FDA批准Alpha DaRT治疗复发性胶质母细胞瘤的IDE申请
FDA 已批准一项试验设备豁免 (IDE) 申请,用于启动一项试点研究,评估 Alpha 扩散型 α 发射体放射治疗 (DaRT) 技术对复...
查看详情 FDA 授予 Paige 突破性设备称号
FDA 授予 Paige 突破性设备称号
Paige PanCancer Detect 获得了 FDA 突破性设备称号,这是 AI 首次跨组织识别多种癌症。...
查看详情 FDA 批准 ALX2004 的新药试验申请
FDA 批准 ALX2004 的新药试验申请
一项评估 ALX2004 在EGFR阳性实体瘤中的单药剂量递增和剂量扩展 1 期试验预计将于 2025 年中期开始。...
查看详情 Ajovy 正在接受儿童发作性偏头痛预防药物审查
Ajovy 正在接受儿童发作性偏头痛预防药物审查
如果获批扩大儿科适应症,AJOVY 将成为首个用于预防成人偏头痛和儿科患者发作性偏头痛的降钙素基因相关肽 (CGRP)...
查看详情 BIIB080 获 FDA 快速通道认证用于治疗阿尔茨海默病
BIIB080 获 FDA 快速通道认证用于治疗阿尔茨海默病
接受高剂量 BIIB080 治疗的患者在第 100 周的整体临床痴呆评定量表总和、简易精神状态检查认知量表和功能活动问卷上...
查看详情 FDA 预计将于 2025 年 5 月做出药品审批决定
FDA 预计将于 2025 年 5 月做出药品审批决定
处方药使用者付费法案(PDUFA) 日期是指美国食品药品管理局(FDA)规定的审查 新药申请(NDA) 或 生物制品许可申...
查看详情 FDA 加速批准 Vanrafia®(阿曲生坦)
FDA 加速批准 Vanrafia®(阿曲生坦)
III 期数据显示,与安慰剂相比,Vanrafia 使蛋白尿减少了 36.1%(P<0.0001),第 6 周即出现改善并持续至第 36 周,且安全...
查看详情 Uplizna获FDA批准用于治疗免疫球蛋白G4相关疾病
Uplizna获FDA批准用于治疗免疫球蛋白G4相关疾病
与安慰剂相比,Inebilizumab 显著降低了治疗和 AC 确定的 IgG4-RD 发作风险 87%。...
查看详情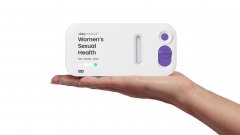 FDA 授权首个衣原体、淋病和滴虫病家庭检测产品
FDA 授权首个衣原体、淋病和滴虫病家庭检测产品
该批准基于一项涉及 2203 名 14 岁及以上女性的临床研究。...
查看详情